
教科書等に載っている電池と電気分解は「図」がよく似ていますが、通常「電池」を学んだあとに「電気分解」を学ぶので、仕組みをよく理解しないと誤解を招きます。
よくある質問として、「電池では⊖から⊕ー電子が流れるのに、電気分解では⊕から⊖に流れるのは何故ですか」
⊝とか⊕とか言っている時点で、非常に曖昧で、⊝を陰極、⊕を陽極として質問されることもよくあります。「用語」を正しく使わないと混乱のもとです。
電解質溶液に「電極」が浸してあります。[?]の部分に何があるかで内容が異なります。
電球やモータなどがつないであれば、電池の図、外部電源や電池記号があれば電気分解です。
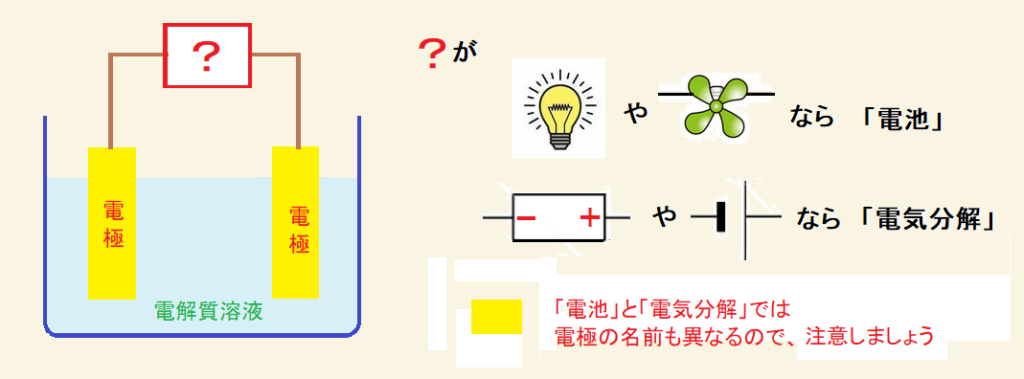
どちらになるかで、「電極」呼び方、「電子の流れ」も違ってきます。
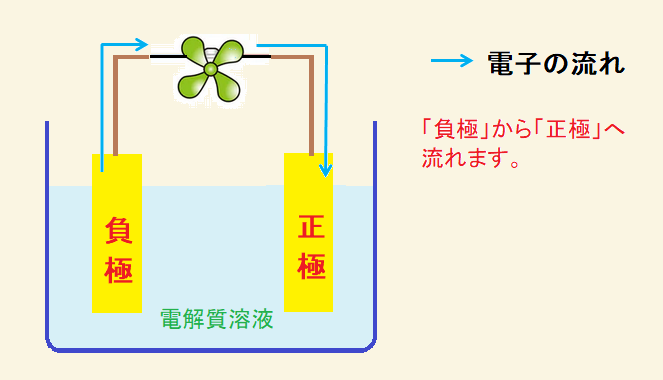
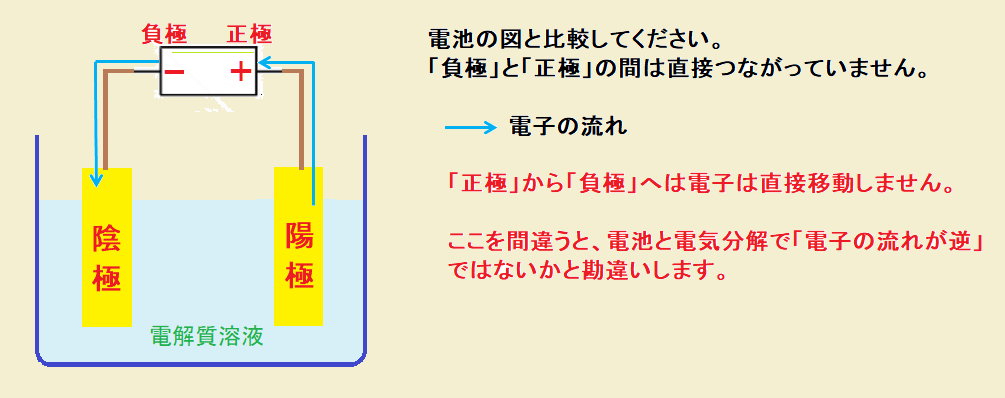
電解質溶液の中は、「イオンが移動」して全体として電気が流れます。
「電子」と「イオン」を混同してはいけません。
ちょっと見ると、「電子の流れ」が逆に見えます。しかし、よく見ましょう。
「陰極」と「負極」、「正極」と「陽極」をしっかり区別して見ましょう。
⊝極とか⊕極のイメージだけで見てはいけません。
どちらも、「負極」から「電子が出て」最終的に「正極」に戻るのです。
直接つながっていないところは「イオン」が手助けしているのです。
